آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
صفحة 1 من اصل 1 • شاطر
 آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
السؤال الأول :
أولاً : اختر الإجابة الصحيحة لكل عبارة مما يلى :
1- يتفاعل البنزين مع الكلور فى ضوء الشمس المباشر مكوناً ¼¼
أ- سيكلوهكسان . ب- هكسان عادى . ج- جامكسان . د- كلورو بنزين .2- القانون الذى يدرس العلاقة بين سرعة التفاعل الكيميائى وتركيز المتفاعلات اكتشفه العالم ¼¼
أ- لوشاتيليه . ب- أفوجادرو . -G جاى لوساك . د- جولدبرج وفاج .3- كمية الكهرباء اللازمة لترسيب ذرة جرامية من الألمونيوم فى التفاعل . Al+3 + 3e- ® Al يساوى ¼
أ- 0.5 فاراداى ب- فاراداى . ج- فاراداى . د- 0.3 فاراداى .4- غاز الأكسجين ¼¼
أ- 32 جرام . ب- 6.02 × 2310 جزئ -G 2 (6.02 × 2310 ) ذرة- يشغل 22.4 لتراً فى stp د- جميع ما سبق .
5- الرقم الهيدروجينى لخمض الهيدروكلوريك 001, مول / لتر يساوى ¼¼
أ- 3 ب- 1 -G ( -3) – 11ثانياً : أ- قارن بين كل مما يأتى :
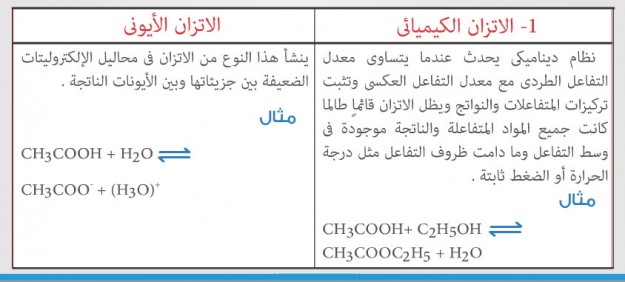
1- الاتزان الكيميائى والاتزان الأيونى . 2- بلمرة بالإضافة وبلمرة بالتكاثف .
3- قانون أفوجادرو وقانون جاى لوساك . 4- الخلية الجافة وخلية الزئبق .



ب- اكتب أسماء المركبات الآتية حسب نظام الأيوباك .


ثالثاً : أ- اكتب الرمز الاصطلاحى ، العامل المؤكسد ، العامل المختزل ، احسب القوة الدفعة الكهربية
فى الخلية الجلفانية الآتية : H20 + Cu+2 ® 2H+ + Cu0علماً بأن جهد أكسدة النحاس = -34, فولت.
ب- اشرح باختصار ما يلى : معدل التفاعل الكيميائى والعوامل التى تؤثر عليه .
ب- معدل التفاعل الكيميائى : هو مقدار التغير فى تركيز المواد المتفاعلة فى وحدة الزمنيتأثر معدل التفاعل (سرعته) بعدد من العوامل هى :
1- طبيعة المواد المتفاعلة : نوع الترابط فى المواد المتفاعلة إذا كانت المواد المتفاعلة أيونية يكون التفاعل سريع ولحظى بينما إذا كانت المواد المتفاعلة تساهمية يكون التفاعل بطئ .
2- تركيز المواد المتفاعلة : تلعب درجة تجزئة المادة دوراً مهماً فى زيادة سرعة التفاعل فكلما زادت عدد الجزيئات المتفاعلة كلما زادت فرص التصادم وزادت سرعة التفاعل .
3- درجة حرارة التفاعل : زيادة درجة الحرارة للتفاعل يزيد نسبة الجزيئات المنشطة وبالتالى يزيد معدل التفاعل الكيميائى .
4- زيادة الضغط أو التبريد على تفاعل غازى متزن تجعله ينشط فى الاتجاه الذى يقل فيه الحجم .
لتحميل الدرس بصيغة PDF اضغط هنا..
 رد: آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
رد: آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
السؤال الثانى :
أولاً : أ- اكتب المفهوم العلمى فى كل من العبارات الآتية :
1- تفاعل الأحماض العضوية مع الكحولات فى وجود مادة نازعة للماء .2- القطب الذى تحدث عنده أو له عملية الأكسدة فى الخلايا الكهروكيميائية .
3- عند ثبوت درجة الحرارة فإن درجة التأين ( ) تزداد بالتخفيف .
4- التحليل الكيميائى الذى يستخدم فى التعرف على مكونات المادة .
5- الكحولات التى ترتبط فيها مجموعة الكاربينول بذرتى كربون وذرة هيدروجين واحدة .
6- كمية الكهرباء اللازمة لترسيب أو ذوبان أو فصل أو تصاعد الكتلة المكافئة الجرامية لأى عنصر بالتحليل الكهربى
7- مادة ألدهيدية عديدة الهيدروكسيل تحتوى على ست ذرات كربون .
8- ظاهرة وجود عدة مركبات عضوية تختلف عن بعضها فى الخواص الفيزيائية والكيميائية وبالتالى
فى الصيغة البنائية ولكنها تشترك فى صيغة جزيئية واحدة .
الإجابة:
1- تفاعل الأسترة .2- الآنود .
3- قانون استفالد للتخفيف.
4- التحليل الكيفى .
5- كحولات ثانوية .
6- الفاراداى .
7- الجلوكوز 8- المشابهة الجزيئية .
ثانياً : أ- باستخدام المعادلات الكيميائية الرمزية والموزونة كيف تحصل على :
1- الفينول من البنزين العطرى . 2- الإيثيلين جليكول من الإيثيلين .
3- T.N.T من بنزوات صوديوم . 4- الجامكسان من حمض الكربوليك
5- الأسيتون من 1- بروبين .



ب- ما دور كل مما يأتى ¼ ؟ :
1- القنطرة الملحية فى الخلايا الجلفانية .
2- حمض الكبريتيك : أ- بطارية السيارة . ب- تفاعل الأسترة . -G إضافة الماء إلى الأيثيلين .
3- الجير الصودا فى تحضير الميثان معملياً .
4- برمنجانات البوتاسيوم فى تفاعل باير .
5- الكيمياء التحليلية فى الزراعة والطب .
(1) القنطرة الملحية فى الخلايا الجلفانية :عبارة عن أنبوبة زجاجية على هيئة حرف U تملأ بمحلول إلكتروليتى لا تتفاعل أيوناته معأيونات محاليل نصفى الخلية ولا مع مواد أقطاب الخلية الجلفانية وتقوم
1- بالتوصيل بين محلولى نصفى الخلية .
2- تمنع الاتصال المباشر بين المحلولين .
3- تقوم بمعادلة الشحنات الموجبة والسالبة التى تتكون فى محلولى نصفى الخلية .
4- تكون فرق الجهد بين محلولى نصفى الخلية .
(2) حمض الكبريتيك : 1- فى بطارية السيارة : كإلكتروليت
2- فى تفاعل الأسترة : كعامل نازع للماء ( لمنع التفاعل العكسى )
3- إضافة الماء إلى الإيثيلين : كوسط حمضى ( لزيادة تركيز H+ )
(3) الجير الصودا فى تحضير الميثان معملياً :
أ- لخفض درجة انصهار مخلوط التفاعل . ب- امتصاص بخار الماء (كعامل نازع للماء)
(4) برمنجانات البوتاسيوم فى تفاعل باير : كعامل مؤكسد (لتكوين الأكسجين الذرى )
(5) الكيمياء التحليلية فى : أ- فى الزراعة : إمكانية معرفة تركيب التربة والصخور لتحديد صلاحيتها للزراعة .
ب- فى الطب : 1- قياس كمية المكونات الفعالة فى الدواء .
2- قياس تركيز السكر فى الدم والبول .
ثالثاً :
أ- مخلوط من كلورات البوتاسيوم وثانى أكسيد المنجنيز كتلته 10 جرام سخن بشدة وبعد انتهاء
التفاعل تبقى منه 8 جرام احسب كتلة ثانى أكسيد المنجنيز تبعاً للتفاعل الآتى :
2KClO3 2KCl + 3O2
ب- هيدروكربون كتلته الجزيئية 58 جرام ويحتوى المول منه على 48 جرام كربون
1- اكتب الصيغة الجزيئية لهذا المركب .
2- للهيدروكربون أيزوميران اكتب الصيغة البنائية لكل منهما مع تسمية كل منهما بنظام الأيوباك .


لتحميل الدرس بصيغة PDF اضغط هنا..
 رد: آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
رد: آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
السؤال الرابع : أولاً : أ- رتب المركبات الآتية :
1- C6H5OH , HCl , CH3COOH , C2H5OH تصاعدياً حسب الخاصية الحامضية .2- NH4Cl , CH3COONa , KCl تصاعدياً حسب قيمة PH
3- اثير ثنائى الميثيل ، حمض الأستيك ، الإيثانول تصاعدياً حسب درجة الغليان .
ب- النحاس النقى 99% يحتوى على نسبة من الشوائب
وضح كيف يمكن تنقيته من الشوائب للحصول على نحاس نقاوته 99.95%
خطوات تنقية النحاس :
1- يوصل الجسم المراد تنقيته بالقطب الموجب للبطارية ( أى يصبح كمصعد ) بعد تنظيفه جيداً .2- يوصل الجسم النقى ( والذى من نفس أيونات الفلز المراد تنقيته بالقطب السالب ) ( أى يصبح كمهبط )
3- يوضع إلكتروليت يحتوى على أيونات الفلز المراد تنقيته


ثانياً : أ- اكتب المعادلة الكيميائية لتحضير غاز الأستيلين فى المعمل مع رسم جهاز التحضير ولماذا يمرر غاز الأستلين أولاً على محلول كبريتات النحاس فى وجود حمض الكبريتيك المخفف قبل جمعه ثم اكتب المعادلة الكيميائية التى توضح تفاعل غاز الأستلين مع وفرة من غاز بروميد الهيدروجين .
ثانيا : رسم جهاز تحضير غاز الأستيلين معملياً
المعادلة الكيميائية : CaC2 + 2H2O C2H2 + Ca (OH)2
يمرر غاز الأستيلين على محلول كبريتات النحاس المحمضة للتخلص من غاز الفوسفين PH3 وغاز كبريتيد الهيدروجين H2S الناتجين من الشوائب الموجودة فى كربيد الكالسيوم تفاعل غاز الأستلين مع وفرة من غاز HBr


ب- احسب عدد الأيونات التى تنتج عن ذوبان 7.1 جرام من كبريتات الصوديوم فى الماء .
-اكتب الصيغة البنائية لكل من :
1- النفتالين . 2- ثنائى الفينيل . 3- وهل يعتبر المركبان أيزوميران ولماذا ؟

ثالثاً : إذا كانت كتلة عينة من كبريتات النحاس المتهدرته ( H2O × CuSO4 , ) هى 10 جرام
وسخنت تسخيناً شديداً إلى أن ثبتت كتلتها فوجدت 6.4 جرام . احسب :
1- النسبة المئوية لماء التبلر فى كبريتان النحاس المتهدرته .
2- عدد جزيئات ماء التبلر .
3- الصيغة الجزيئية للملح المتهدرت .


لتحميل الدرس بصيغة PDF اضغط هنا..
 رد: آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
رد: آخر مراجعات كايرو دار فى الكيمياء للثانوية العامة 2015
السؤال الخامس : أولاً : كيف تميز عملياً بين كل من :
1- غاز الميثان وغاز الأيثيلين .2- حمض الكربوليك وحمض الإيثانويك .
3- الإيثانول و2- ميثيل – 2 – بروبانول .
الإجابة:
| 1- التجربة | غاز الميثان | غاز الإثيلين |
| أ- بإضافة البروم المذاب فى رابع كلوريد الكربون إلى كل منهما | لا يتأثر | اختفاء (زوال) اللون الأحمر للبروم |
| ب- بإضافة برمنجانات البوتاسيوم فى وجود وسط قلوى إلى كل منهما | لا يتأثر | اختفاء (زوال) اللون البنفسجىC2H4 + H2O |
 | ||
| 2- التجربة | حمض الكربوليك (الفينول) | حمض الإيثانويك (حمض الخليك) |
| أ- بإضافة ملح كربونات أو بيكربونات الصوديوم إلى كل منهما | لا يتأثر | حدوث فوران وتصاعد غاز CO2الذى يعكر ماء الجير الرائق |
 | ||
| ب- بإضافة قطرات من محلول كلوريد الحديد IIIإلى كل منهما | يتكون لون بنفسجى | لا يتأثر |
| 3- التجربة | الإيثانول (كحول أولى) | 2- ميثيل -2- بيوتانول (كحول ثالثى) |
| بإضافة محلول برمنجانات البوتاسيوم المحمضة (بحمض الكبريتيك المركز إلى كل منهما | زوال (اختفاء) اللون البنفسجى لبرمنجانات البوتاسيوم مع تصاعد رائحة الخل فى النهاية | لا يتأثر |
 | ||
ثانياً : أ-اكتب التفسير العلمى لكل مما يأتى :
1- لا توجد أيونات هيدروجين موجبة ( بروتونات ) حرة فى المحاليل المائية للأحماض .2- يعتبر بطارية السيارة من الخلايا الجلفانية الثانوية .
3- لا يعتبر العامل الحفاز مؤثراً على التفاعلات الانعكاسية التى فى حالة اتزان .
4- يستعاض عن الكريوليت باستخدام مخلوط من أملاح فلوريدات كل من الألمونيوم والصوديوم
والكالسيوم عند استخلاص الألمونيوم من البوكسيت بالتحليل الكهربى .
5- لا يستخدم دليل الفينولفثالين عند الكشف عن الأحماض .
الإجابة:
1- لأنه ينجذب إلى زوج الإلكترونات الحر الموجود على ذرة الأكسجين لأحد جزيئات الماء ويرتبط معه برابطة تناسقية ويعرف هذا البروتون ( بالبروتون المماه ) أو أيون الهيدرونيوم ويرمز له بالرمز
2- لأنها تتميز بأن تفاعلاتها الكيميائية تفاعلات انعكاسية وتختزن الطاقة الكهربية على هيئة طاقة كيميائبة والتى يمكن تحويلها مرة أخرى إلى طاقة كهربية عند اللزوم ( ويمكن إعادة شحنها بإمرار تيار كهربى من مصدر للتيار الكهربى المستمر له جهد أكبر قليلاً من الجهد الناتج من بطارية السيارة مما يؤدى إلى حدوث تفاعل عكس التفاعل التلقائى )
3- لأنه يزيد من سرعة كلا الاتجاهين الطردى والعكسى ويقلل الزمن اللازم للوصول إلى حالة الاتزان دون أن يغير من موضع الاتزان .
4- حيث يعطى هذا المخلوط من البوكسيت مصهوراً يتميز بـ :
أ- انخفاض درجة انصهاره .
ب- انخفاض كثافته مقارنة بالمصهور مع معدن الكريوليت وانخفاض كثافة المصهور يسهل فصل الألمونيوم المنصهر والذى
يكون راسباً فى قاع خلية التحليل الكهربى .
5- لأنه يكون عديم اللون فى الوسط الحمضى
ب-يتم استخلاص الألمونيوم بالتحليل الكهربى للبوكسيت.وضح بالمعادلات اللاتينية ما يلى :
1- تفاعل الأكسدة عند الآنود . 2- تفاعل الاختزال عند الكاثود .3- التفاعل الكلى الحادث . 4- تفاعل الأكسجين المتصاعد عند أقطاب الكربون .
الإجابة:

ج - احسب حاصل الإذابة Ksp لملح فوسفات الكالسيوم Ca3 (PO4)2 شحيح الذوبان فى الماء علماً بأن تركيز أيونات الكالسيوم 1 × 10-4 مول / لتر وتركيز أيونات الفوسفات هى 5 × 10-3 مول / لتر .
الإجابة:

ثالثاً : أ -من التفاعل الكيميائى الآتى :

احسب كتلة وحجم وكثافة وعدد ذرات وعدد جزيئات غاز الأكسجين التى تنتج من التحلل الحرارى 24 جرام كلورات البوتاسيوم .
الإجابة:

ب- اذكر استخداماً واحداً لكل من :
1- الهالوثان . 2- بولى بروبلين . 3- الهيدروميتر .الإجابة:
1-الهالوثان : تستخدم حالياً كمخدر بأمان تام وصيغته CHBrClCF32-بولى بروبلين : تستخدم فى السجاد – المفارش – الشكائر البلاستيك – المعلبات
3- الهيدرويتر : جهاز يستخدم لقياس كثافة السوائل .
لتحميل الدرس بصيغة PDF اضغط هنا..
 مواضيع مماثلة
مواضيع مماثلة» مراجعة الكيمياء العضوية للثانوية العامة طبعة 2015 الجديدة للأستاذ حسام سويفى
» مراجعات كايرو دار فى الكيمياء للصف الثالث الثانوى
» اختبار مميز وجديد على الكيمياء العضوية للثانوية العامة 2015
» الكيمياء الكهربية للثانوية العامة 2015 للأستاذ سيد الزويدى فى ملف 56 ورقة وورد
» 2 نموذج اختبار شامل منهج الكيمياء للثانوية العامة 2015 للأستاذ محمود عطية
» مراجعات كايرو دار فى الكيمياء للصف الثالث الثانوى
» اختبار مميز وجديد على الكيمياء العضوية للثانوية العامة 2015
» الكيمياء الكهربية للثانوية العامة 2015 للأستاذ سيد الزويدى فى ملف 56 ورقة وورد
» 2 نموذج اختبار شامل منهج الكيمياء للثانوية العامة 2015 للأستاذ محمود عطية
صفحة 1 من اصل 1
صلاحيات هذا المنتدى:
لاتستطيع الرد على المواضيع في هذا المنتدى
 الرئيسية
الرئيسية
